Wiki BIOSYSTEM
Шикима́тный путь — метаболический путь, промежуточным метаболитом которого является шикимовая кислота (шикимат). Шикиматный путь отмечается как специализированный путь биосинтеза бензоидных ароматических соединений (очень часто в этом качестве наряду с шикиматным путём отмечается также поликетидный (ацетатно-малонатный) механизм построения бензольных ядер — замыкание (zip-сборка) ароматических систем посредством внутримолекулярной конденсации по типу кротоновой). Шикиматным путём в природе синтезируются такие известные соединения, как фенилаланин, тирозин, триптофан, бензоат, салицилат. Шикиматный путь является источником ароматических предшественников терпеноидных хинонов (убихинонов, пластохинонов, менахинонов, филлохинонов), токоферолов, фолата, флавоноидов, лигнинов, суберинов, меланинов, таннинов и огромного множества других соединений, играющих в природе различную роль. Шикиматный путь — один из древнейших эволюционно консервативных метаболических путей; как источник фундаментальных составляющих (в первую очередь — трёх протеиногенных аминокислот) живой материи фактически представляет собой часть первичного метаболизма. Значение шикиматного пути велико, так как этот путь является единственным установленным путём биосинтеза ряда важнейших природных соединений, в том числе значимых в плане их практического использования. В строгом смысле под шикиматным путём следует понимать только общую часть разветвлённого метаболического процесса — путь биосинтеза хоризмовой кислоты (хоризмата).
История открытия и изучения
В 1935 году немецкий химик-органик Германн Отто Лауренц Фишер (1888—1960) и Герда Дангшат (?—1964) отметили, что структурно охарактеризованные ими кислоты хинная и шикимовая могут быть биогенетически (метаболически) тесно связанными с бензоидными ароматическими соединениями, в частности, с галловой кислотой. Для хинной кислоты была известна биологическая ароматизация (при участии микроорганизмов наблюдали образование из хинной кислоты некоторых фенольных соединений, а также было показано, что хинная кислота в организме млекопитающих метаболизируется в гиппуровую кислоту). Однако всё же чёткого подтверждения того, что гидроароматические кислоты являются естественными предшественниками природных ароматических соединений, не существовало до 1950-х годов.

В 1950 году американский микробиолог Бернард Дэвис (1916—1994), применяя ультрафиолетовое облучение, используя свой оригинальный метод отбора с применением пенициллина, получил серию мутантов Escherichia coli, способных расти лишь в такой питательной среде, в которую добавлялись ароматические соединения. Многие мутанты нуждались в фенилаланине, тирозине, триптофане, пара-аминобензоате и пара-гидроксибензоате (в следовых количествах). Неожиданно оказалось, что потребность во всех пяти соединениях можно удовлетворить добавлением шикимовой кислоты (шикимата), в то время считавшейся редким соединением, встречающимся лишь у некоторых растений. Другая группа полученных Дэвисом мутантов не отвечала на добавляемый шикимат как на заменяющий ароматические соединения фактор роста, и обнаружилось, что некоторые из этих мутантов сами накапливали в культуральной среде шикимовую кислоту. Мутанты разных групп могли синтрофно расти на минимальной питательной среде.
Таким образом, шикимат, который отнюдь не является ароматическим соединением, оказался промежуточным продуктом в процессах биосинтеза трёх ароматических протеиногенных аминокислот, пара-аминобензоата и других существенных ароматических соединений. Очевидно, у некоторых полученных Дэвисом мутантов был нарушен синтез шикимата, тогда как у других мутантов были блокированы более поздние стадии метаболического процесса.
При помощи ауксотрофных мутантов Escherichia coli, Aerobacter aerogenes и Neurospora crassa и с применением изотопно-меченых соединений был прослежен весь путь от углеводных предшественников до первичных и вторичных метаболитов ароматической природы. Промежуточные соединения удавалось обнаружить и изолировать благодаря тому, что определённые мутанты их накапливали. Эксперименты с мутантами и выделяемыми ими соединениями позволяли выстраивать эти соединения в цепочку и отмечать в этой цепочке места недостающих метаболитов. Установить начальные этапы пути, связывающие его с известными путями, было значительно сложнее. Мутантный штамм Escherichia coli, накапливающий в культуральной среде шикимовую кислоту, выращивали на средах, содержащих в качестве единственного источника углерода C-меченую по определённым позициям d-глюкозу или другие соединения. После этого шикимовую кислоту выделяли. Распределение радиоактивных меток определялось путём ступенчатой химической деструкции. Анализ полученных результатов привёл к выводу, что три из семи атомов углерода молекулы шикимовой кислоты приходят из гликолиза, остальные четыре — из пентозофосфатного пути. Природа исходных соединений была выяснена, когда стал доступен синтетический d-эритрозо-4-фосфат. Было показано, что клеточные экстракты Escherichia coli легко конвертируют d-эритрозо-4-фосфат и фосфоенолпируват в дегидрохиннат. Сначала предположили, а затем экспериментально установили, что промежуточным соединением является семиуглеродный продукт конденсации — соединение, которое теперь известно как ДАГФ. Также, при помощи радиоизотопных меток было показано, что экспериментально наблюдаемое почти количественное превращение под действием бактериальных клеточных экстрактов d-седогептулозо-1,7-дифосфата в дегидрошикимат или шикимат не может быть объяснено преобразованием цельной молекулы, без промежуточного расщепления её на C4 и C3-фрагменты.
Важнейшая часть работы по расшифровке пути была проделана Бернардом Дэвисом (важные пионерские работы по выяснению метаболических путей при помощи мутантов велись под его руководством в им же основанной и возглавляемой научно-исследовательской лаборатории туберкулёза при Корнеллском медицинском колледже, Манхэттен, Нью-Йорк) в сотрудничестве с исследователями из Колумбийского университета — Дэвидом Спринсоном (1910—2007) и Паритхичери Сринивасаном (1927—2012). В числе других сотрудников — Масаюки Катажири, Ульрих Вайс, Элизабет Мингиоли, Иван Саламон, Джудит Левин. Значительный вклад в изучение отдельных стадий процесса внесли также австралийцы Франк Гибсон (1923—2008), Джеймс Питтард и многие другие исследователи. Полная картина метаболического пути стала ясна в 1962—1964 годах, когда Франк Гибсон наконец выделил и изучил долго ускользавшую от наблюдения субстанцию «compound X» — недостающий промежуточный метаболит, структура которого до этого уже была предсказана (впоследствии подтверждена Ллойдом Джэкмэном при помощи ЯМР-спектроскопии). По предложению своего тестя это соединение Гибсон назвал хоризматом (хоризмовой кислотой). Гипотеза Дэвиса (5-карбоксивинил-шикимат-3-фосфат, или, как его тогда называли, «Z1-phosphate», — предшественник как фенилаланина, тирозина, так и триптофана) была доказана, гипотеза Спринсона (последний общий предшественник трёх ароматических аминокислот — фосфошикимовая кислота) подтверждения не получила.
В 1950-х годах был, как описано выше, установлен путь биосинтеза дегидрохинната через ДАГФ, долго считавшийся единственным. В геномную эру стали накапливаться факты, которые требовали объяснения. Наиболее любопытным было то, что во многих геномах не выявлялось ортологов генов биосинтеза дегидрохинната при наличии ортологов генов его дальнейшего метаболизма. Результаты последовавших исследований метаболических возможностей организмов подтвердили предположения о существовании альтернативного пути биосинтеза дегидрохинната. В 2004 году были опубликованы результаты исследований американского биохимика Роберта Уайта по расшифровке пути биосинтеза дегидрохинната через ADTH. Однако предложенная Уайтом гипотетическая схема биосинтеза DKFP (прекурсор ADTH) впоследствии не подтвердилась. В 2006 году Роберт Уайт и Сюй Хуэйминь сообщили, что им удалось выяснить истинный путь биосинтеза DKFP у Methanocaldococcus jannaschii.
Название пути
Название «шикиматный путь» (the shikimate pathway), также можно встретить «путь шикимовой кислоты» (the shikimic acid pathway), было определено исторически (изучение началось с установления метаболической роли шикимовой кислоты, см. выше). В 1979 году Флос (H. G. Floss), желая подчеркнуть ключевую роль и мультипотентность другого важнейшего промежуточного соединения (хоризмата), предложил название «the chorismate pathway». Ввиду того, что хоризмат находится хотя и в важнейшей, но не единственной точке ветвления цепочки химических превращений, и в силу того, что старое название к тому времени уже хорошо закрепилось, подобное переименование было признано контрпродуктивным и от него отказались. Другое возможное название, «the aromatic pathway», также было отвергнуто, так как многие ароматические соединения синтезируются иными путями, некоторые же неароматические продукты синтезируются из шикиматных предшественников, минуя стадию ароматизации.
Годы открытия основных соединений смотри в приложении.
Распространённость и локализация
Шикиматный путь осуществляется в клетках прокариот (как бактерий, так и архей) и эукариот (грибов, растений, всевозможных протистов, но не животных). У растений реакции шикиматного пути проходят в цитозоле и, практически независимо, в пластидах (главным образом в хлоропластах), однако гены практически всех ферментов локализованы в ядре; при нормальных условиях роста около 20 % всего усваиваемого растением углерода протекает этим путём, в масштабе биосферы по некоторым оценкам это составляет около 7×10 тонн в год. У организмов, клетки которых не содержат пластиды, шикиматный путь протекает в цитозоле. Многоклеточные животные (Metazoa) не имеют ферментной системы шикиматного пути, так как получают протеиногенные ароматические аминокислоты и прочие необходимые продукты шикиматного пути в достаточном количестве с пищей (или от симбионтов) и потому эволюцией освобождены от необходимости их биосинтеза de novo. С другой стороны, избавившись от «лишнего» ещё на этапе своего эволюционного становления, животные попали в зависимость от ряда экзогенных соединений (незаменимые аминокислоты, значительная часть витаминов). Животные способны преобразовывать готовые ароматические продукты шикиматного пути, в частности, способны превращать незаменимую аминокислоту фенилаланин в тирозин, являющийся заменимой аминокислотой при условии достаточного поступления фенилаланина с пищей. Шикиматный путь частично или полностью утрачен также некоторыми микроорганизмами, живущими исключительно в богатых необходимыми веществами средах.
У бактерий три реакции, завершающие биосинтез фенилаланина, могут проходить как в цитозоле, так и в периплазматическом пространстве или экстрацеллюлярно.
Начальные этапы шикиматного пути
В настоящее время известно два пути биосинтеза дегидрохинната — предшественника шикимата. Это классический путь через ДАГФ и обнаруженный позже у архей путь через ADTH.
Путь через ДАГФ
Наиболее распространённым в органическом мире и первым изученным путём образования дегидрохинната является путь его биосинтеза из d-эритрозо-4-фосфата и фосфоенолпирувата. d-Эритрозо-4-фосфат образуется преимущественно в системе транскетолазных и трансальдолазных реакций окислительного и восстановительного пентозофосфатных путей, а также, у некоторых микроорганизмов, — при участии фосфокетолазы. Фосфоенолпируват образуется в процессе гликолитического распада углеводов и из оксалоацетата, а у ряда организмов — также одностадийно из пирувата. Сначала происходит взаимодействие по типу альдольной конденсации d-эритрозо-4-фосфата и фосфоенолпирувата с образованием семи́углеродного соединения 3-дезокси-d-арабино-гепт-2-улозонат-7-фосфат (ДАГФ, англ. DAHP, множество синонимов). Осуществляющий эту реакцию фермент — ДАГФ-синтаза (КФ 2.5.1.54) — представлен, как правило, несколькими изоформами; известно 2 класса. Далее ДАГФ претерпевает внутримолекулярную альдольную конденсацию (циклизацию), что даёт дегидрохиннат. Реакцию осуществляет фермент 3-дегидрохиннат-синтаза (КФ 4.2.3.4), требующая в качестве кофермента NAD, который участвует в механизме реакции, потому как во время каталитического акта сначала происходит окисление гидроксильной группы при C5-атоме углерода молекулы ДАГФ в карбонильную, а в дальнейшем — восстановление этой карбонильной группы обратно в гидроксильную (механизм, характерный и для других циклаз фосфорилированных углеводов ). Считается, что в реакцию ДАГФ вовлекается в полукетальной α-пиранозной форме (на схеме из некоторых соображений приведена только формула открытой кето-формы ДАГФ).

Описанный путь биосинтеза дегидрохинната характерен для бактерий, эукариот и части архей.
Путь через ADTH
У многих архей (в основном представители типа Euryarchaeota, относимые к классам Archaeoglobi, Halobacteria, Methanomicrobia, Methanobacteria, Methanococci, Methanopyri, а также типа Thaumarchaeota) активность ДАГФ-синтазы не была показана, а при исследовании их геномов не удалось выявить каких-либо ортологов генов ДАГФ-синтазы. Не было обнаружено и ортологов генов известного класса 3-дегидрохиннат-синтазы. Впоследствии выяснилось, что биосинтез дегидрохинната у этих организмов осуществляется другим путём. В экспериментах на Methanocaldococcus jannaschii установлено, что исходными соединениями служат d-глицеральдегид-3-фосфат, дигидроксиацетонфосфат, l-аспартат-4-се́миальдегид. d-Глицеральдегид-3-фосфат и дигидроксиацетонфосфат (глицерон-фосфат) образуются в клетке разными путями, в том числе в системе транскетолазных, трансальдолазных реакций и в ходе гликолитического распада углеводов. l-Аспартат-4-семиальдегид, также как и названные триозофосфаты, не является специфическим соединением данного метаболического пути; образуется восстановлением β-карбоксильной группы l-аспартата, является предшественником ряда протеиногенных аминокислот (метионина, треонина, изолейцина, а также лизина в одной из двух известных стратегий его биосинтеза). Отщепление фосфата от d-глицеральдегид-3-фосфата генерирует пирувальдегид (метилглиоксаль), который под влиянием фруктозо-1,6-дифосфат-альдолазы класса I (фермент с достаточно низкой субстратной специфичностью) конденсируется с дигидроксиацетонфосфатом (вступает в реакцию в свободном виде либо в виде других субстратов альдолазы — d-фруктозо-1-фосфата или d-фруктозо-1,6-дифосфата) с образованием 6-дезокси-5-кетофруктозо-1-фосфата (сокр. англ. DKFP). DKFP далее под влиянием другой родственной неспецифической альдолазы (КФ 4.1.2.13 / 2.2.1.10) взаимодействует с l-аспартат-4-семиальдегидом с образованием 2-амино-3,7-дидезокси-d-трео-гепт-6-улозоната (сокр. англ. ADTH, синоним: 2-амино-2,3,7-тридезокси-d-ликсо-гепт-6-улозонат). Последнее соединение окислительно дезаминируется и циклизуется в дегидрохиннат под влиянием NAD-зависимого фермента дегидрохиннат-синтазы-II (КФ 1.4.1.24).

Итак, возникающий в результате циклизации шестичленный карбоцикл в дальнейшем подвергается ароматизации (в большинстве случаев).
Дальнейшие превращения дегидрохинната
Дегидрохиннат может обратимо восстанавливаться NAD-, NADP- и PQQ-зависимыми дегидрогеназами в хиннат, роль в биосинтезе ароматических соединений которого обсуждается (у некоторых растений уже выявлен фермент хиннат-гидролиаза, дегидратирующий хиннат в шикимат, что создаёт возможность превращения дегидрохинната в шикимат через хиннат, а не только через дегидрошикимат путём, описанным ниже). Однако строго доказано, что на пути к предшественникам важнейших ароматических соединений если не необходимым, то по крайней мере основным (у всех хорошо изученных в этом отношении организмов) этапом является обратимая дегидратация (фермент: 3-дегидрохиннат-дегидратаза (КФ 4.2.1.10), стереохимия — 1,2-син-элиминирование для ферментов типа I и 1,2-анти-элиминирование в случае ферментов типа II) дегидрохинната в дегидрошикимат. У ряда организмов дегидрошикимат окисляется NADP-зависимой дегидрогеназой в 3,5-дидегидрошикимат или под влиянием 3-дегидрошикимат-дегидратазы (КФ 4.2.1.118) может обратимо дегидратироваться в ароматическое соединение протокатехат (через эти стадии может идти образование галлата, пирокатехина, пирогаллола, флороглюцина, гидроксигидрохинона, прочих фенолов). Но на пути к наиболее важным ароматическим соединениям дегидрошикимат должен претерпеть ряд других химических изменений. Дегидрошикимат обратимо восстанавливается NAD-, NADP- и PQQ-зависимыми дегидрогеназами в шикимат, далее следует необратимая киназная реакция (фермент: шикимат-киназа (КФ 2.7.1.71), макроэргический донор фосфорильной группы — ATP). Образовавшийся шикимат-3-фосфат (фосфошикимат) взаимодействует с фосфоенолпируватом и образуется 5-карбоксивинил-шикимат-3-фосфат (фермент: ЕПШФ-синтаза, англ. EPSP synthase (КФ 2.5.1.19)). Две последние реакции рассматриваются как подготовительные для последующих реакций элиминирования, необходимых для завершения π-электронного секстета бензольного кольца (ароматизации). Необратимая реакция элиминирования фосфат-аниона даёт хоризмат (фермент: хоризмат-синтаза (КФ 4.2.3.5) — флавопротеид, кофактором является FMNred либо FADred, бифункциональные хоризмат-синтазы обладают к тому же NADred или NADPred-зависимой флавин-редуктазной активностью). Стереохимически реакция происходит как 1,4-анти-элиминирование, что предполагает механизм более сложный (предположительно радикальный, принимая во внимание структурные особенности субстрата и характер кофакторов), чем простое синхронное сопряжённое элиминирование, иначе происходило бы нарушение правил орбитальных взаимодействий. В строгом смысле, собственно шикиматный путь образованием хоризмата завершается. От хоризмата расходятся по крайней мере семь путей, ведущих к ароматическим соединениям и родственным им хинонам (в приведённом ниже общем обзоре этих путей отражена основная биосинтетическая роль шикиматного пути).

Гидроксибензойная
кислота
П р и м е ч а н и е к р и с у н к у: На схеме отмечены различные возможные биохимические превращения, обычно не все из которых реализуются в конкретных организмах. Отмечены наиболее важные биохимические превращения, но разнообразие возможных превращений не ограничивается лишь этими. Хотя некоторые отмеченные на схемах здесь и далее реакции принципиально обратимы (обратимость реакций отмечена в соответствии с KEGG Pathway), равновесие в физиологических условиях может быть практически нацело смещено в определённую сторону, что обусловлено термодинамическими и другими факторами. Каноническая часть шикиматного пути размещена в верхней трети рисунка. Маленькой красной стрелочкой указана та стадия, которую блокирует глифосат (ЕПШФ-синтазная реакция).
В узком смысле шикиматный путь — каскад из 7-ми ферментативных реакций, приводящий к образованию хоризмата — общего предшественника ряда важнейших соединений. Краткая информация по этим реакциям сведена в таблицу, которая вынесена в приложение
Пути, расходящиеся от хоризмата
В живой природе выявлено не менее семи различных путей, расходящихся от хоризмата и приводящих к ароматическим соединениям, а также родственным им хинонам:
- через префенат к фенилаланину, тирозину, фенилпропаноидам и другим соединениям.
- через антранилат к индолу, триптофану и другим соединениям.
- через 2-амино-4-дезоксихоризмат к пигментам и антибиотикам феназинового ряда.
- через 4-амино-4-дезоксихоризмат к пара-аминобензоату, фолату, хлорамфениколу и другим соединениям.
- через пара-гидроксибензоат к убихинону и другим соединениям.
- через изохоризмат к структурным производным нафталина (нафтохинонам), салицилату и другим соединениям.
- через футалозин к нафтохинонам и, возможно, к другим соединениям.
Известны и другие превращения хоризмата, например, присутствующая в его структуре эфирная связь может подвергаться гидролизу. Это путь к алициклическому соединению (1R,3R,4R)-3,4-дигидроксициклогексан-1-карбоксилату (предшественник-стартер в биосинтезе рапамицина, такролимуса, аскомицина и др.). Аналогично может начинаться биосинтез циклогексилкарбонил-КоА (предшественник асукамицина, селамектина, ансатриенина A, ω-циклогексил-жирных кислот и других соединений).
Путь через префенат
Изомеризация хоризмата в префенат происходит в результате [3,3]-сигматропной перегруппировки, по типу напоминающей перегруппировку Кляйзена (в более широком смысле — является перегруппировкой Кляйзена). Эта реакция способна происходить спонтанно (термически), подкисление среды и нагревание ускоряют её. Фермент хоризматмутаза (КФ 5.4.99.5) в физиологических условиях ускоряет реакцию в 2•10 раз.
Реакция дегидратационного декарбоксилирования (механизм — сопряжённое элиминирование) префената приводит к фенилпирувату. Эта реакция способна проходить спонтанно (термически, кислая среда является сильным катализатором), для её ускорения существуют ферменты: специфическая префенатдегидратаза (КФ 4.2.1.51) и неспецифическая карбоксициклогексадиенилдегидратаза (КФ 4.2.1.91). Обратимое переаминирование фенилпирувата приводит к протеиногенной аминокислоте фенилаланину.
Окислительное декарбоксилирование (окислитель — NADox или NADPox, ферменты — префенатдегидрогеназы) префената приводит к 4-гидроксифенилпирувату, обратимое переаминирование которого приводит к протеиногенной аминокислоте тирозину.
Известен также путь к фенилаланину и тирозину через арогенат (претирозин). Арогенат получается в результате переаминирования префената. Дегидратационное декарбоксилирование арогената приводит к фенилаланину, а окислительное декарбоксилирование (окислитель — NADox или NADPox) арогената приводит к тирозину. У зелёных растений и цианобактерий путь биосинтеза фенилаланина и (или) тирозина через арогенат обычно является преобладающим.
У некоторых организмов (мутанты Neurospora crassa и др.) найдены спиро-арогенат (лактамное производное арогената) и d-префениллактат (восстановленное по карбонилу производное префената), которые также склонны к ароматизации.
У многих организмов, в том числе у животных и человека, есть фермент аэробная тетрагидробиоптерин-зависимая фенилаланин-4-монооксигеназа (синоним: фенилаланин-4-гидроксилаза, КФ 1.14.16.1), осуществляющий однонаправленное гидроксилирование фенилаланина в тирозин.

Фенилпируват, 4-гидроксифенилпируват, фенилаланин, тирозин и продукты их обмена дают начало огромному множеству различных ароматических соединений (фенилпропаноиды, катехоламины, различные пептиды, многие алкалоиды (изохинолиновые, тропановые, протоалкалоиды), многие гликозиды (кумариновые, большинство известных цианогенных), коферменты PQQ и F420, лигнины, меланины и множество прочих). 4-Гидроксифенилпируват окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат, являющийся предшественником токоферолов, пластохинона. Бензоат, пара-гидроксибензоат, салицилат, протокатехат, фанилацетат, гидрохинон могут быть продуктами биодеградации соединений, синтезированных через префенат, помимо чего пара-гидроксибензоат, салицилат и гидрохинон могут быть синтезированы из хоризмата другими путями.
Путь через антранилат
Антранилат синтезируется из хоризмата ферментом антранилатсинтазой (КФ 4.1.3.27). Донором аминогруппы выступает амидный азот глутамина либо аммоний. Антранилат является предшественником индола и протеиногенной аминокислоты триптофана.
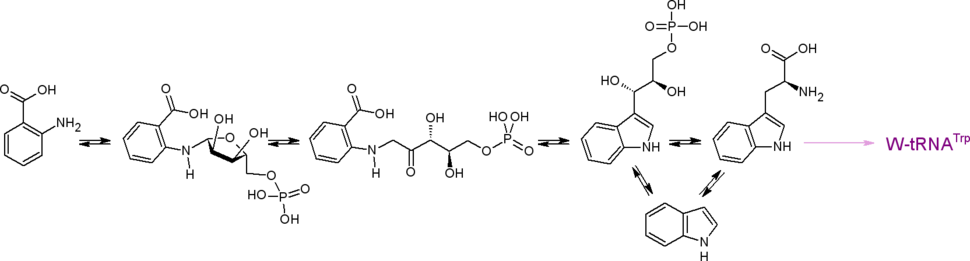
Три последних названных соединения являются предшественниками очень многих соединений: индольных, хинолиновых, хиназолиновых, акридоновых алкалоидов, бензоксазиноидов и др. К примеру, антранилат служит предшественником так называемых pyo-соединений (структурные производные хинолина, такие, как псевданы и N-меркапто-4-формилкарбостирил), индол — прекурсор индикана, а из триптофана синтезируется антибиотик пирролнитрин. Пирокатехин (катехол) образуется в результате декарбоксилирования протокатехата, а также может быть синтезирован из антранилата, из салицилата.
Путь через антранилат близок к пути через 2-амино-4-дезоксихоризмат; эти пути рассматриваются как самостоятельные, так как антранилат и 2-амино-4-дезоксихоризмат производятся из хоризмата разными ферментами.
Путь через 2-амино-4-дезоксихоризмат
Фермент 2-амино-4-дезоксихоризмат-синтаза (КФ 2.6.1.86) производит из хоризмата 2-амино-4-дезоксихоризмат (2-амино-2-дезоксиизохоризмат, сокр. англ. ADIC), открывая путь к структурным производным феназина. Донором аминогруппы выступает амидный азот глутамина. Далее происходит ферментативный гидролиз эфирной связи 2-амино-4-дезоксихоризмата, что даёт (5S,6S)-6-амино-5-гидроксициклогекса-1,3-диен-1-карбоксилат, который далее под влиянием фермента (КФ 5.3.3.-) изомеризуется в (1R,6S)-6-амино-5-кетоциклогекса-2-ен-1-карбоксилат. Последнее соединение подвергается диагонально-симметричной димеризации — в результате — получается предшественник с предобразованной структурой феназиновых соединений. Результатом дальнейших метаболических превращений этого соединения у бактерий является образование пигментов и антибиотиков феназинового ряда, в том числе незамещённого феназина, жёлтого феназин-карбоксилата, 2-гидроксифеназина, синего нефлуоресцирующего пигмента с антибиотической активностью пиоцианина (Pseudomonas aeruginosa), сафенамицинов, эсмеральдинов (димерные феназины).

Различные наборы феназиновых соединений производятся разнообразными бактериями (Pseudomonas, Streptomyces, Nocardia, Sorangium, Brevibacterium, Burkholderia, Erwinia, Vibrio, Pelagiobacter, Brevibacterium, Pantoea agglomerans и др.), среди архей феназиновые соединения найдены у Methanosarcina. Феназиновый оперон (phz-оперон) обычно содержит ген phzC. Этот ген кодирует ДАГФ-синтазу класса II, которая структурно сильно отличается от регулируемых аминокислотами ДАГФ-синтаз, относимых к классу I (прокариотическая ДАГФ-синтаза PhzC структурно ближе к ДАГФ-синтазам высших растений (они также относятся к классу II), чем к прокариотическим ДАГФ-синтазам класса I (AroF, AroG, AroH), которым гомологичны ДАГФ-синтазы дрожжей). Так как phz-оперон содержит отдельный ген с ДАГФ-синтазной функциональностью, то очевидно, что обмен феназинов способен оказывать сильное регуляторное влияние на весь шикиматный путь.
Феназиновые соединения являются структурными производными хиноксалина (бензпиразина). Также, определённые структурные производные хиноксалина могут синтезироваться из триптофана.
Известен флавопротеид (содержит FMN, КФ 1.3.99.24), который окисляет 2-амино-4-дезоксихоризмат в 3-(карбоксивинилокси)-антранилат, включающийся в структуру некоторых ендииновых антибиотиков в процессе их биосинтеза. Прекурсоры ендииновых антибиотиков могут образовываться также и через антранилат.
Путь через 4-амино-4-дезоксихоризмат
Изомерный антранилату пара-аминобензоат синтезируется из хоризмата через 4-амино-4-дезоксихоризмат (сокр. англ. ADC) ферментом пара-аминобензоат-синтазой (КФ 2.6.1.85 + КФ 4.1.3.38). Донором аминогруппы выступает амидный азот глутамина. пара-Аминобензоат является предшественником коферментов ряда фолата (THF, THMPT и др.). пара-Аминобензоат и его метаболические производные являются стартерными единицами в биосинтезе некоторых антибиотиков (кандицидин-D, хачимицины (трихомицин), леворин и др.), остаток пара-аминобензоата входит в состав антибиотиков пликацетин, норпликацетин, амицетин, бамицетин и др. Окислением аминогруппы пара-аминобензоата генерируется пара-нитробензоат, который в составе тиоэфира с коферментом A является предшественником-стартером в биосинтезе ауреотина. Спонтанный или ферментативный гидролиз эфирной связи 4-амино-4-дезоксихоризмата приводит к (3R,4R)-4-амино-3-дигидроксициклогекса-1,5-диен-1-карбоксилату. У некоторых микроорганизмов выявлен фермент, катализирующий аналогичную хоризматмутазной [3,3]-сигматропную перегруппировку 4-амино-4-дезоксихоризмата в 4-амино-4-дезоксипрефенат. Эта реакция составляет этап биосинтеза непротеиногенной аминокислоты пара-аминофенилаланин. пара-Аминофенилаланин — прекурсор нескольких известных антибиотиков, из него образуются 4-(диметиламино)-фенилаланин (остаток входит в структуру некоторых циклических пептидных антибиотиков, например, пристинамицина-IA),пара-нитрофенилсеринол (предшественник хлорамфеникола).

Путь через пара-гидроксибензоат
Хоризмат-пируват-лиаза (КФ 4.1.3.40) катализирует реакцию элиминирования пирувата из хоризмата, что приводит к пара-гидроксибензоату. Это не единственный способ биосинтеза пара-гидроксибензоата, который может также образовываться из фенилаланина и тирозина через пара-кумарат (растения, животные, многие бактерии). пара-Гидроксибензоат является предшественником убихинона, растительных гликозидов, шиконина и прочих соединений.

Путь через изохоризмат
Хоризмат-гидроксимутаза (изохоризмат-синтаза, КФ 5.4.4.2) осуществляет обратимую изомеризацию хоризмата в изохоризмат. Изохоризмат является предшественником салицилата, 2,3-дигидроксибензоата (пирокатехата) (предшественник сидерофорных соединений, таких, как энтеробактины), орто-сукцинилбензоата (предшественник менахинонов, филлохинонов, а также ализарина, лавсона, юглона, люцидина, дунниона, моллугина), множества прочих соединений. Из изохоризмата салицилат синтезируется путём элиминирования пирувата (основной, но не единственный способ биосинтеза салицилата). Известен как перициклический, так и не перициклический механизмы этой реакции, описано оба соответствующих типа ферментативной активности. У некоторых организмов известен фермент (изохоризмат-мутаза), катализирующий [3,3]-сигматропную перегруппировку изохоризмата в изопрефенат. Из изопрефената образуются непротеиногенные аминокислоты мета-карбоксифенилаланин и мета-карбокситирозин — вторичные метаболиты высших растений (Nicotiana silvestris, Iris sp. и др.). Изопрефенат — наиболее вероятный предшественник 3-формилтирозина, найденного у Pseudoalteromonas tunicata.

кислота
Футалозиновый путь
Биоинформатический анализ секвенированных геномов привёл к обнаружению у некоторых прокариот (Streptomyces spp., Helicobacter pylori, Campylobacter jejuni) другого пути от хоризмата к менахинонам. В начале этого пути в ходе ферментативной реакции из хоризмата, инозина (аденозина) и фосфоенолпирувата образуется футалозин (аминодезоксифуталозин).
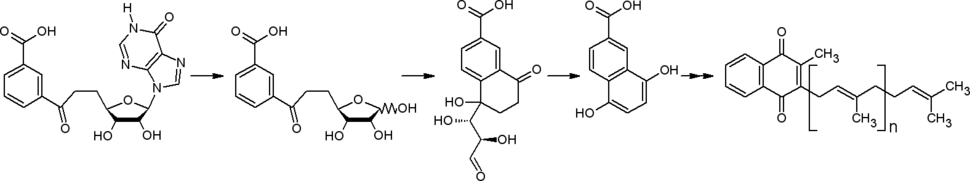
При синтезе менахинонов через изохоризмат и по футалозиновому пути наблюдается разный характер включения в структуру групп атомов, составляющих скелеты исходных соединений (в этих путях второй (хиноидный) карбоцикл достраивается к карбоциклу хоризмата с разных сторон).
Неароматические продукты шикиматного пути
Шикиматный путь является специализированным путём биосинтеза ароматических соединений, но может быть рассмотрен как источник ряда неароматических. В основном это соединения, образующиеся из ароматических продуктов шикиматного пути в результате утраты ими ароматичности. Примером может служить диен-изоцианидный антибиотик (продуцирует Trichoderma hamatum), предшественником которого является тирозин:

Ещё пример: фенилацетат (продукт метаболических превращений фенилпирувата и фенилаланина) — биосинтетический предшественник некоторых структурных производных циклогептана (ω-циклогептил-жирных кислот).
В других случаях бензольные кольца шикиматного происхождения могут утрачивать ароматичность без разрушения или перестройки углеродного скелета. Так, Rhodopseudomonas palustris способен утилизировать ароматические соединения, в частности деароматизует бензоат, в фототрофных анаэробных условиях гидрируя его до циклогекс-1-ен-1-карбоксилата (дальнейшая утилизация последнего способна покрывать потребность клетки в углероде). Цианобактериальный дипептид радиозумин, состоит из модифицированных остатков аминокислот, предположительно являющихся метаболическими производными пара-аминофенилаланина с частично гидрированными кольцами. В то же время установлено, что собственные биосинтетические пути разнообразных неароматических структурных производных ароматических аминокислот, таких как 2,5-дигидрофенилаланин, 2,5-дигидротирозин, тетрагидрофенилаланин, тетрагидротирозин, 2,5-дигидростильбен, 2-карбокси-6-гидроксиоктагидроиндол (структурный компонент цианобактериального пептида эругинозина),антикапсин (предшественник бацилизина), исходят от префената. Известен фермент, префенат-декарбоксилаза, участвующий в синтезе этих соединений и декарбоксилирующий префенат без сопутствующей дегидратации или окисления, что позволяет избежать ароматизации, характерной для более известных метаболических превращений префената.Кетомицин (антибиотик алициклической структуры) также образуется из префената.
Известны также неароматические продукты, синтезируемые из относительно ранних промежуточных неароматических соединений шикиматного пути. В качестве примера таких продуктов можно назвать микоспорины (микоспорин-подобные аминокислоты), которые обнаруживаются в таксономически разнообразных морских, пресноводных и наземных организмах. Один из метаболических путей, приводящих к микоспоринам, ответвляется от шикиматного пути на уровне дегидрохинната. Существование этого пути установлено в экспериментах с аскомицетом Trichothecium roseum. Другой выявленный (цианеи: Nostoc punctiforme, Chlorogloeopsis sp.) путь биосинтеза микоспоринов не использует промежуточные соединения шикиматного пути, но протекает с участием 2-эпи-5-эпи-валиолон-синтазы — гомолога 3-дегидрохиннат-синтазы. Исходным соединением является d-седогептулозо-7-фосфат — центральный метаболит, соединение, имеющее определённые черты структурного сходства с ДАГФ.

кислота
(пиранозная форма)
(общая формула)
Известны также продукты взаимодействия ароматических продуктов шикиматного пути с неароматическими промежуточными соединениями шикиматного же пути. Так, 5-O-кофеоилшикимат (дактилифрат) и 3-O-кофеоилшикимат (неодактилифрат) представляют собой шикимовую кислоту, у которой C5-гидроксил (или, соответственно, C3-гидроксил) этерифицирован остатком ароматической кофейной кислоты. Известными производными хинната аналогичного строения являются хлорогенат и неохлорогенат.

Термодинамический аспект
Термохимия и кинетика отдельных реакций шикиматного пути хорошо изучены. Проводились специальные термодинамические исследования и расчёты. Ниже — данные по отдельным реакциям.
1). Термодинамика ДАГФ-синтазной реакции
ФЕП(aq) + d-Э4Ф(aq) + H2O(1) = ДАГФ(aq) + Ф(aq)
(C3H2O6P)(aq) + (C4H7O7P)(aq) + H2O(l) = (C7H10O10P)(aq) + (HO4P)(aq)
Тепловой эффект реакции (изменение энтальпии системы, молярная энтальпия реакции), измеренный калориметрически при T = 298,15 K, pH = 8,18, Im = 0,090 моль/кг, Tris + HCl буфер; установившейся кажущейся константе равновесия K′ > 1,4•10:
ΔrHm (cal) = −(67,7 ± 1,5) кДж/моль
Расчётная стандартная молярная энтальпия реакции (T = 298,15 K и Im = 0):
ΔrHm = −(70,0 ± 3,0) кДж/моль (~ −17 ккал/моль)
Расчётная стандартная молярная свободная энергия Гиббса реакции (T = 298,15 K и Im = 0):
ΔrGm ≈ −39 кДж/моль
Расчётная (

